Notions de 2nde à maitriser avant le cours : ADN, mutations génétiques
INTRODUCTION
L’alternance des divisions cellulaires et des réplications permet de comprendre comment l’information génétique peut se transmettre à l’identique de cellules en cellules, mais aussi de génération en génération. (voir chapitre 3)
Cela permet d’assurer le maintien des caractéristiques fonctionnelles dans des tissus : toutes les cellules d’un même tissu proviennent d’une même cellule-mère, elles ont donc la même information génétique. (ex : les cellules du duodénum synthétisent toutes la lactase car elles sont issues de la même cellule-mère par mitose et réplication) mais aussi de maintenir les caractéristiques d’une espèce de génération en génération (ex : tous les êtres humains possèdent le gène de la lactase car il est transmis par méiose, réplication et fécondation).
Cependant, il existe bien une variabilité génétique : les allèles (donc les séquences de nucléotides) sont différents chez certains individus, entrainant des différences de phénotypes.
Ces différences sont issues des mutations de l’ADN : des changements de la séquence de nucléotides entrainent des différences d’information génétique, et donc des caractères différents.
–> Comment apparaissent les mutations de l’ADN et quelles en sont les conséquences ?
I- Causes des mutations génétiques
A- Les mutations : des modifications de la séquence d’ADN
Les mutations sont des modifications d’un ou plusieurs nucléotides dans la séquence d’ADN.
Ces mutations peuvent être des insertions (un nucléotide est ajouté à la séquence), des délétions (un nucléotide est retiré de la séquence) ou des substitutions (un nucléotide est remplacé par un autre)
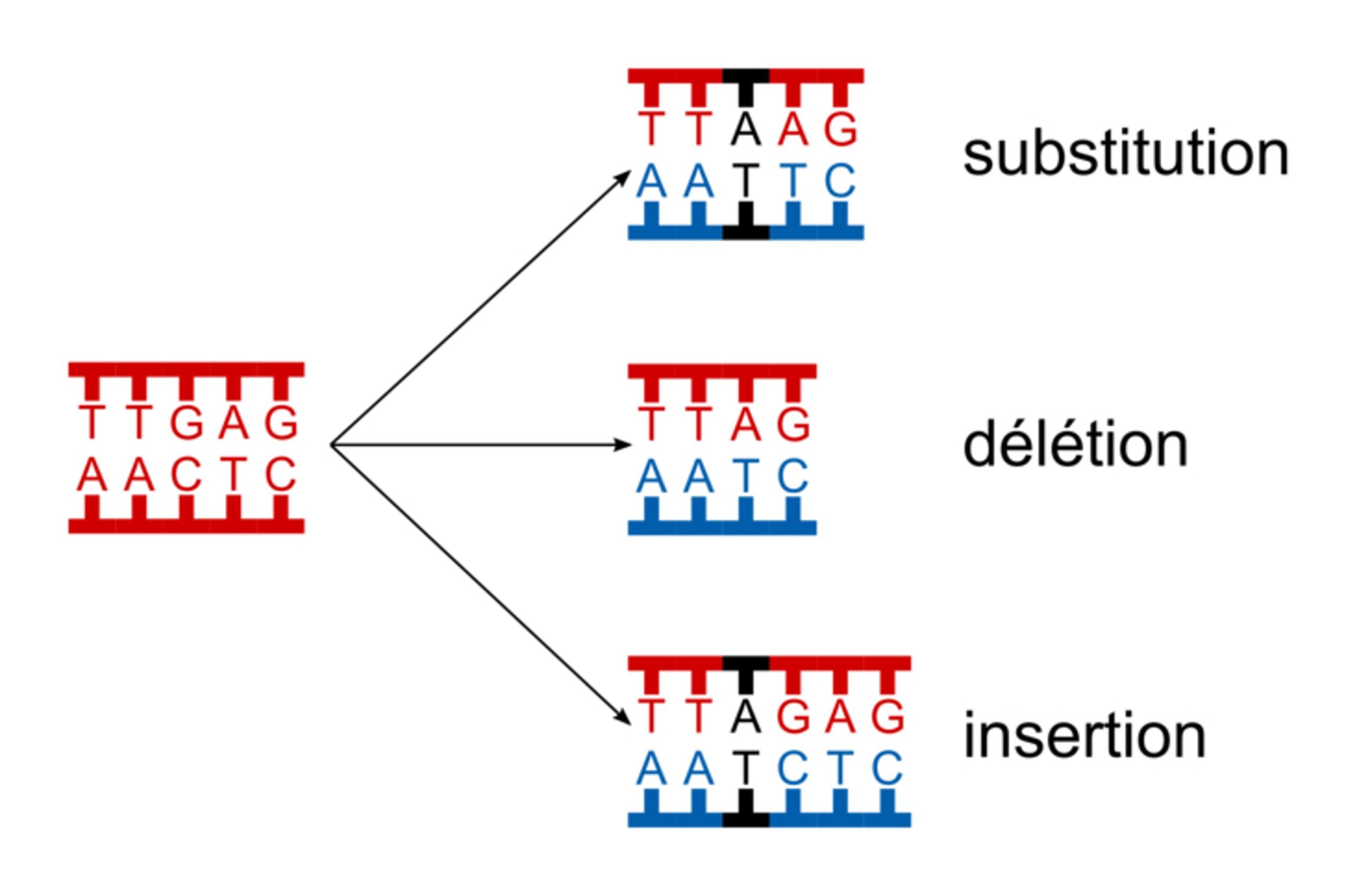
Dans certains cas, la mutation d’un gène peut entrainer la formation d’une protéine différente de la protéine initiale.
Pour cela, il faut que la mutation :
– Touche un gène : ce n’est pas obligatoire car la majorité de l’ADN est non codant
– Entraine le remplacement d’un acide aminé par un autre : ce n’est pas obligatoire car le code génétique est redondant, donc parfois, en changeant 1 nucléotide, on tombe sur le même acide aminé suite à la transcription et la traduction
La formation d’une nouvelle protéine pourra alors modifier le phénotype
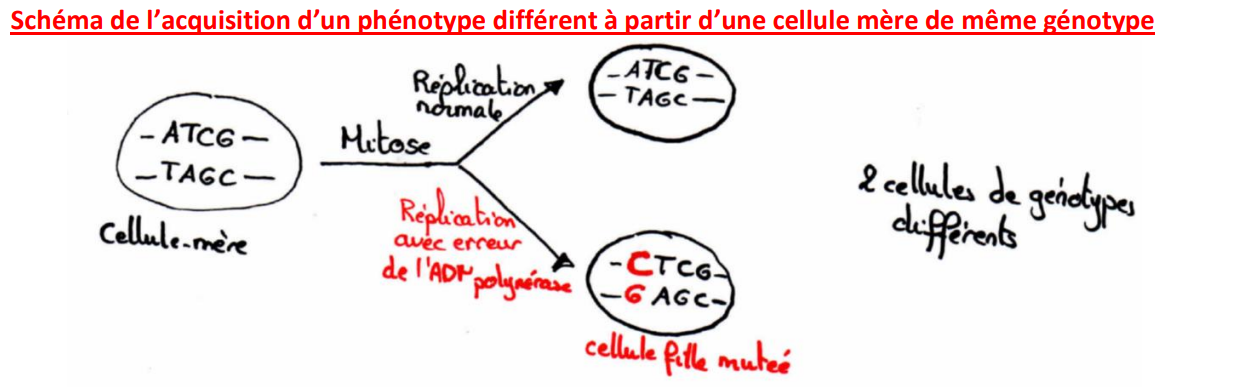
B- Les causes des mutations
Des erreurs peuvent se produire aléatoirement lors de la réplication de l’ADN, lorsque l’ADN polymérase n’apparie pas le bon nucléotide. Cela crée une mutation spontanée et aléatoire.
Activité fréquence de mutation
L’ADN polymérase réalise environ 1 erreur tous les 100 000 nucléotides (taux d’erreur de 10-5), ce qui provoque des mutations spontanées.
Ce taux est augmenté par l’action de facteurs environnementaux, appelés agents mutagènes (tabac, UV, produits chimiques …) qui créent des modifications de l’ADN qui font que l’ADN polymérase se trompe et apparie le mauvais nucléotide.
Remarque : Il existe aussi des mutations induites : on peut provoquer volontairement, en laboratoire, des mutations à des endroits bien précis du génome afin de modifier volontairement le génotype et donc le phénotype → on crée ainsi des OGM nouvelle génération !
L’ADN polymérase a un taux d’erreur de 10-5 nucléotides, cependant, le taux réel de mutation suite à la réplication est plutôt d’une mutation tous les 10 000 000 nucléotides (taux d’erreur de 10-7) : Cela signifie qu’un système de réparation existe.
C- La réparation des erreurs
Les mutations sont relativement rares et elles sont le plus souvent réparées par un ensemble d’enzymes capables de repérer des anomalies dans la structure de l’ADN : elles éliminent la portion anormale et l’ADN polymérase vient combler le brin incomplet.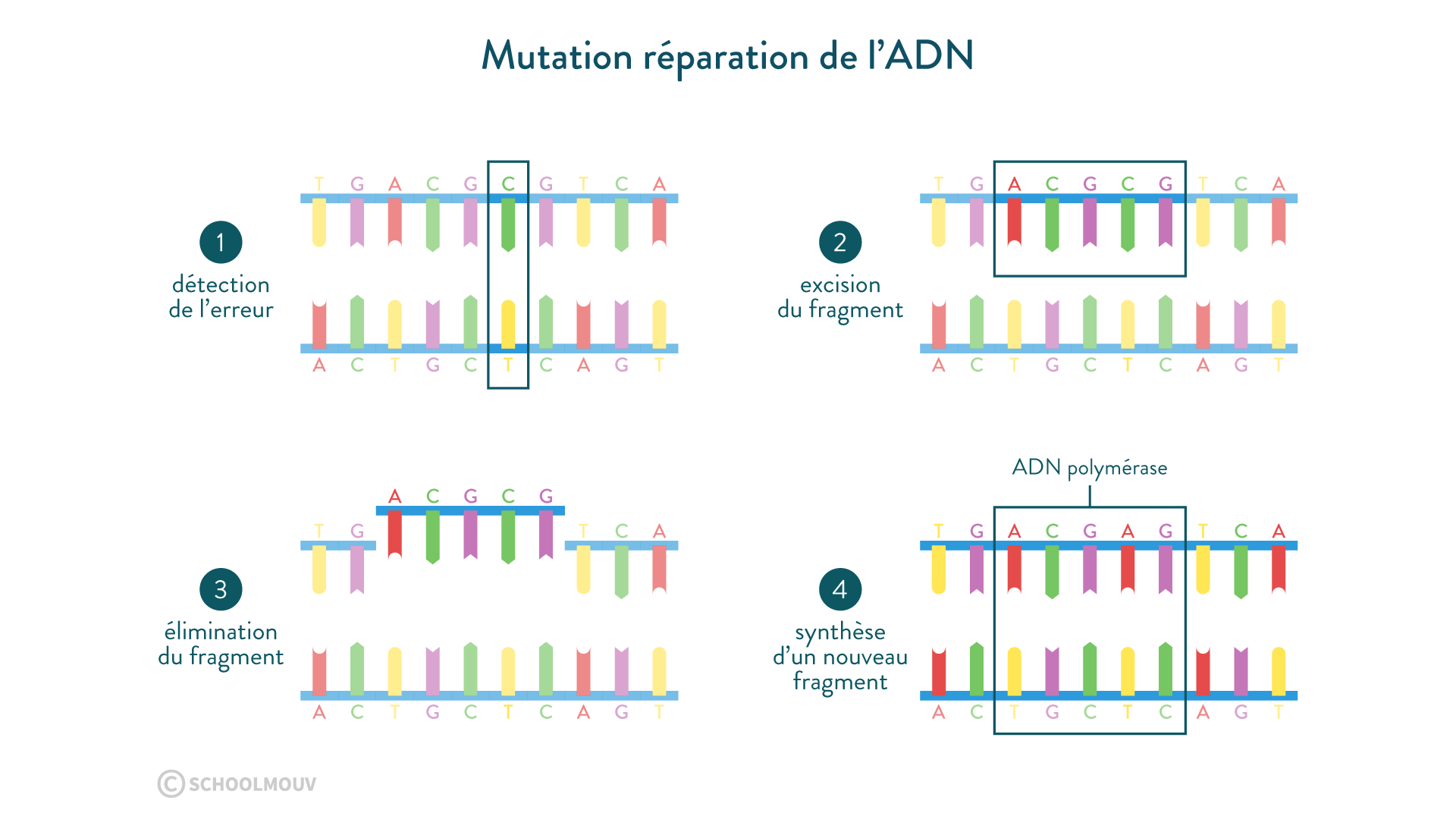
Lorsque ces erreurs ne sont pas réparées, elles persistent dans la cellule après la réplication et seront transmises au moment de la division cellulaire : les cellules filles hériteront donc de cette mutation.
II- Conséquences des mutations somatiques : altération des génomes et cancers
A- Modification du génome d’un clone.
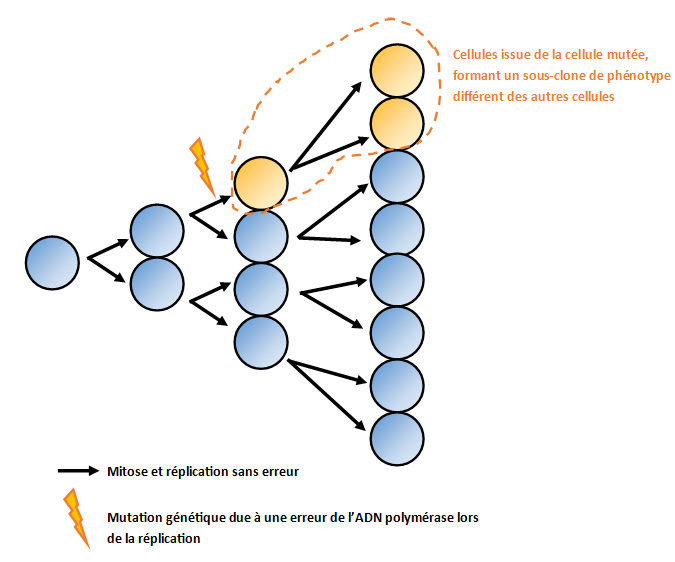
Si une mutation se produit dans une cellule somatique, elle sera transmise par mitose à toutes les cellules filles (= a tout le clone).
Dans ce cas, si la mutation entraine une modification du phénotype, toutes les cellules issues de la cellule mutée par mitose auront le nouveau phénotype.
Cependant, si la mutation a lieu dans une cellule somatique, elle ne sera pas transmissible à la génération suivante donc pas héréditaire.
Exemple : une mutation somatique sur le gène codant pour la protéine mélanine (responsable de la pigmentation de la peau) peut entrainer des taches pigmentaires.
B- Mutations somatiques et cancers
Si la mutation intervient sur un gène responsable de la régulation du cycle cellulaire (c’est-à-dire responsable de la durée des phases G1 et G2), les cellules porteuses de la mutation se diviseront de manière incontrôlée et beaucoup trop rapidement. Cela aboutit à la formation de tumeurs et déclenchera des cancers.
Ainsi les cancers sont dus à des mutations somatiques, qui sont, comme vu précédemment, aléatoires mais favorisées par les agents mutagènes. Se protéger de ces agents mutagènes permet de diminuer le risque de cancer.
Cependant, il existe aussi des susceptibilités génétiques héréditaires aux cancers, ce qui ne peut pas s’expliquer par des mutations somatiques qui ne se transmettent pas à la descendance …
III- Conséquences des mutations germinales : maladies génétiques héréditaires
Si une mutation se produit dans une cellule germinale (cellule de testicule ou d’ovaire) elle pourra être transmise aux gamètes par méiose et donc à la génération suivante par la reproduction sexuée : elle deviendra héréditaire.
L’étude des arbres généalogiques permet de prévoir le risque de transmission de ces maladies dans les générations futures en étudiant la transmission de l’allèle muté.
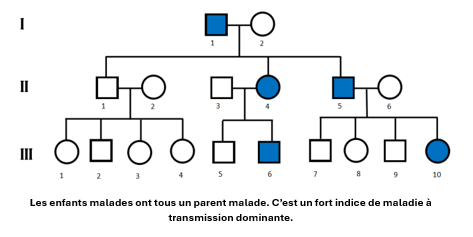
Si la maladie se déclenche lorsqu’un seul allèle muté est présent (donc chez des individus hétérozygotes), elle est dite à transmission dominante : un enfant malade aura alors obligatoirement un parent malade, et le risque de transmission parent-enfant est alors de 50%
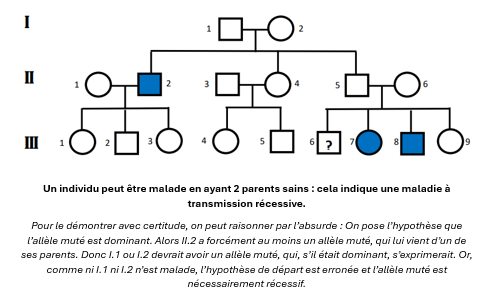
Si la maladie se déclenche uniquement lorsque l’allèle muté est présent en 2 exemplaires (donc uniquement chez des individus homozygotes), elle est dite à transmission récessive : un enfant pourra alors être malade même si ces deux parents ne le sont pas (mais qu’ils sont porteurs sains).
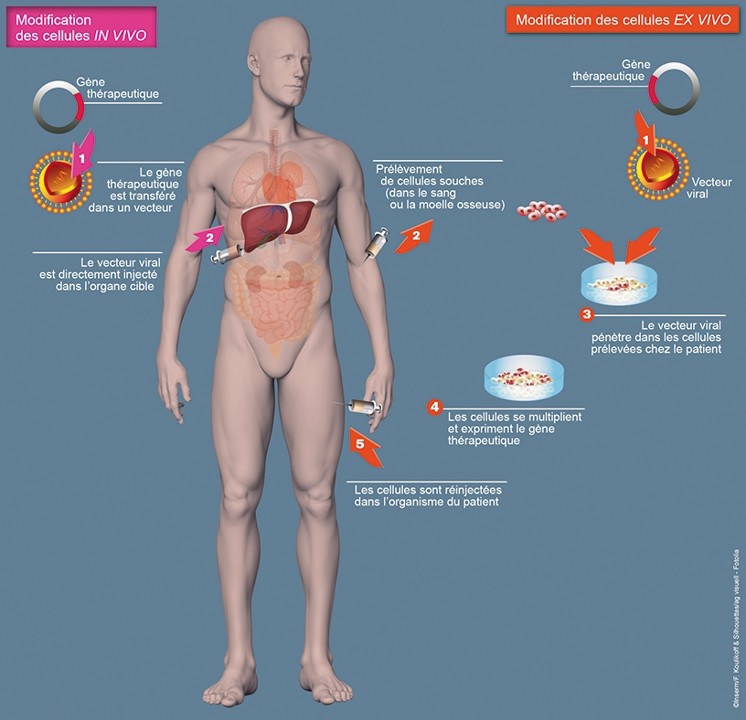
La connaissance des maladies génétique a permis à la médecine de développer des traitements qui soulagent temporairement les symptômes les plus gênants en agissant sur les conditions du milieu. La thérapie génique constitue cependant le seul espoir de guérison totale de la maladie, en remplaçant l’allèle muté par une copie saine.
Les mutations, lorsqu’elles se produisent dans des cellules germinales, peuvent entrainer des maladies génétiques, mais aussi être source d’innovations.
II- Conséquences des mutations à l’échelle des espèces : innovations et évolution
A- Création de nouveaux allèles et évolution des espèces
Rappel de 2nde : Les mutations sont à l’origine de la diversité des allèles au cours du temps. Elles peuvent donc permettre l’apparition de nouveaux variants de caractères et amener une augmentation de la diversité des phénotypes.
Les nouveaux allèles formés par mutation peuvent être plus ou moins transmis aux générations suivantes (en fonction des effets de la sélection naturelle et de la dérive génétique) et participent donc à l’évolution des espèces
Les mutations sont donc à l’origine de la biodiversité.
Activité – Apparition des résistances aux antibiotiques chez les bactéries.
Par exemple, chez les bactéries, des mutations chez un individu peuvent permettre l’apparition de résistance à certains antibiotiques.
Dans ces cas, si les traitements aux antibiotiques sont mal suivis ou trop fréquents, la sélection naturelle entrainera une meilleure conservation de l’allèle muté et la population entière de bactérie peut alors devenir résistante (car les individus porteurs de la mutation sont les seuls à survivre au traitement et se reproduisent donc plus que les individus non porteurs de la mutation). Les antibiotiques ne seront alors plus efficaces.
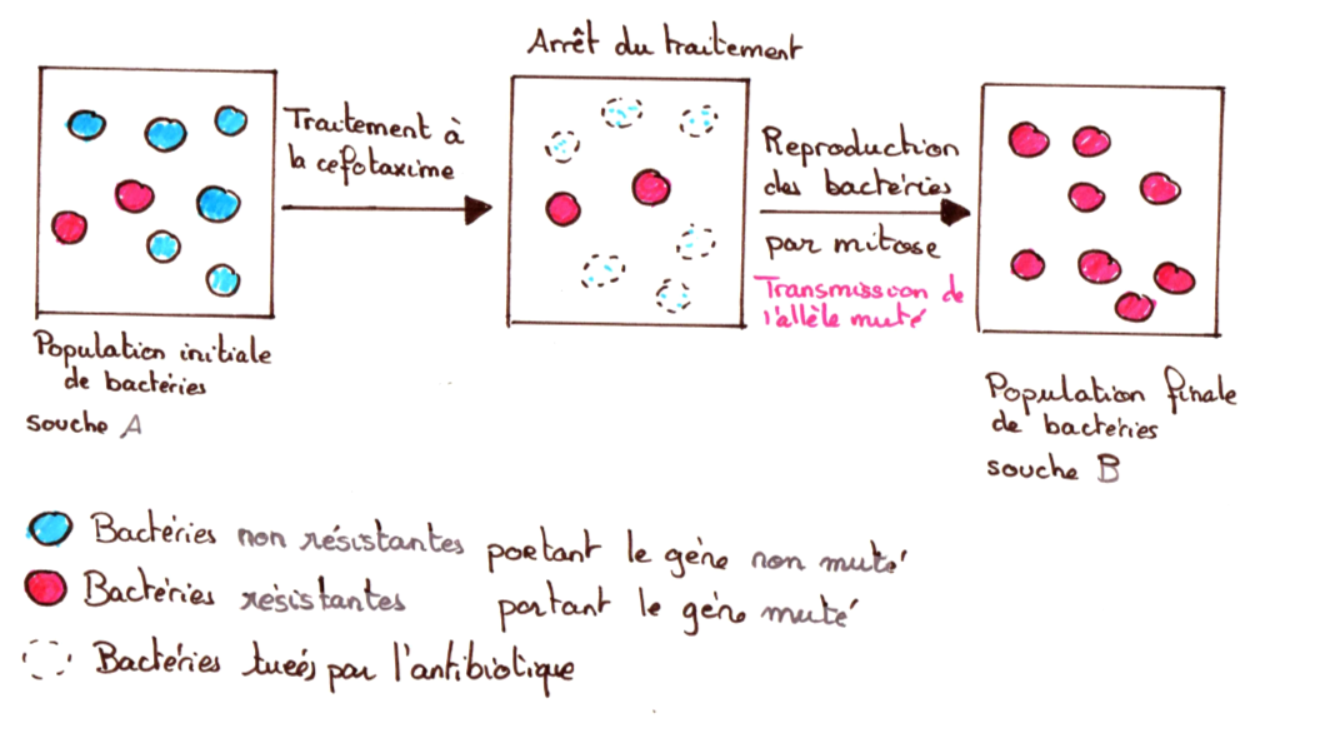
C’est aujourd’hui un important problème de santé publique car il est difficile de trouver de nouveaux antibiotiques.
B- Reconstituer une histoire évolutive en étudiant les mutations du génome
Depuis 2004, le génome humain est entièrement séquencé (cela signifie qu’on connait la séquence de nucléotide de chaque gène humain). Cela a été rendu possible par une collaboration scientifique internationale au sein du projet génome humain.
La connaissance de ces séquences, et la comparaison entre les séquences de différentes populations permettent de reconstituer une partie de l’histoire évolutive de l’homme.
Grâce aux techniques modernes, on peut reconstituer les génomes d’êtres humains disparus à partir de fossiles. En les comparant aux génomes actuels, on peut reconstituer les principales étapes de l’histoire humaine récente.
